近日,专注于研发乙型肝炎病毒(HBV)感染疗法的Spring Bank Pharmaceuticals宣布了正在进行的“ACHIEVE”临床2期试验的第二队列(50mg,单一疗法)的A部分的顶线结果。该公司正在开发通过口服给药的选择性免疫调节剂inarigivir,作为慢性HBV感染患者组合疗法的重要组成药物,目标是以简单、安全和有选择性的方式显著提高功能治愈率。ACHIEVE临床试验的A部分的主要终点是评估药物的安全性和抗病毒活性,其指标是治疗12周时HBV DNA相对于基线的变化,还有多个探索性的次要终点。该队列中的所有患者已经转换为每日300mg,持续12周的富马酸替诺福韦酯(tenofovir disoproxil fumarate)疗法。

全世界大约有2.57亿人感染乙型肝炎病毒(“HBV”),其中包括美国和欧洲约1700万人,该病毒导致肝病进展,每年约有887,000人死亡。目前HBV在研的新疗法相对较少。现有的护理标准需要使用抗病毒疗法的慢性治疗来抑制HBV病毒。虽然已有预防乙型肝炎传染的有效疫苗,但仍需要改善HBsAg清除,以及可能走向治愈的疗法。
该试验的第二队列包含18名可评估的患者,其中14名在inarigivir 50mg治疗组(10例HBeAg阳性,4例HBeAg阴性),4例在安慰剂组。在inarigivir治疗组中,患者对inarigivir耐受性良好,没有出现严重的不良反应。与安慰剂组相比,inarigivir治疗组在第12周时显示出HBV DNA的统计学显著性降低,平均减少0.74 log10(p = 0.0008)。与安慰剂相比,HBeAg阴性患者的HBV DNA平均减少1.05 log10(p = 0.01),HBeAg阳性患者平均减少0.61 log10(p = 0.006)。
该队列的次要终点也显示出积极结果:对于HBV RNA减少这个次要终点,治疗组(平均减少0.95 log10,p = 0.03)也显著优于安慰剂(平均增加0.48 log10),而且HBeAg阴性患者中效果更显著;此外,当比较第一队列(25mg)和第二队列(50mg)的HBV DNA和HBV RNA反应时,第二队列显示出剂量依赖性的下降;对于HBV表面抗原(HBsAg)减少这个次要终点,治疗组中一名HBeAg阳性患者的HBsAg持续减少0.5 log10以上。所有4例HBeAg阴性患者在第12周时均检测不到HBV RNA,但HBsAg未见明显减少,暗示患者的HBsAg可能主要来自于整合型HBV DNA。
当把ACHIEVE试验的第一和第二队列患者组合分析时,将患者通过基线病毒量(以6log10为分界)或者HBsAg水平(以4log10为分界)分组后,对“HBV DNA降低”这个主要终点的分析显示出,初始的基线病毒量与HBV DNA降低之间存在非常显著的正相关性,并与HBeAg状态无关。
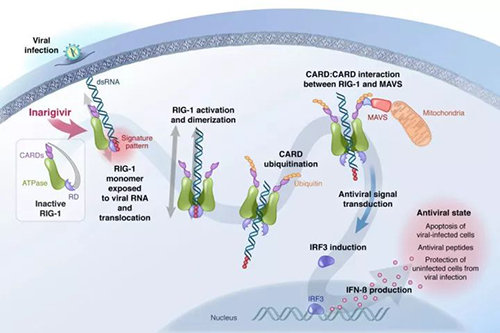
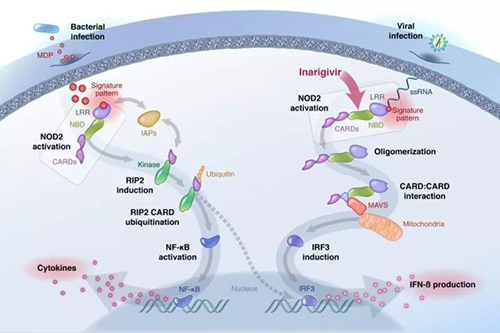
▲ Inarigivir启动双重抗病毒机制:抑制病毒复制,与RIG-I结合的Inarigivir防止病毒聚合酶参与病毒RNA的复制;促进病毒清除,活化的RIG-I诱导内源性IFN产生。(图片来源:Spring Bank Pharmaceuticals官网)
ACHIEVE试验的病毒学核心首席研究员、维多利亚传染病参考实验室(Victorian Infectious Diseases Reference Laboratory)研究及分子开发负责人Stephen Locarnini教授表示:“我们看到了低剂量inarigivir对HBV DNA及HBV RNA所表现出的剂量依赖性的抗病毒效果,这与可能的pgRNA壳体化抑制是一致的,但目前还没看到inarigivir带来的完全免疫反应。”
Spring Bank已经启动ACHIEVE研究A部分的第三队列(100mg)临床试验,并预计在2018年第二季度获得顶线结果。
据了解,Spring Bank已与Gilead Sciences达成了临床合作协议。根据合作,Gilead Sciences需要负责开展一项用于评估inarigivir和替诺福韦艾拉酚胺(商品名为Vemlidy)共同给药的治疗慢性HBV患者的2期试验。与ACHIEVE研究A部分相似,该2期临床的试验方案将包含12周的inarigivir(50mg)和Vemlidy联用治疗的研究,之后所有患者将转为接受12周的Vemlidy单药给药。Spring Bank预计Gilead Sciences将在2018年第一季度开展此项临床试验。
“我们很高兴地宣布,在ACHIEVE试验里对第二队列进行的每日50mg inarigivir,持续12周的测试中,我们达到了安全性和有效性的主要终点,” Spring Bank首席医学官Nezam Afdhal博士表示:“在与完全免疫反应无关的抗病毒剂量的inarigivir治疗下,患者出现的HBV DNA和HBV RNA的反应是令人鼓舞的,这结果支持对其进行进一步的研发,我们正在开发将包括inarigivir的组合疗法作为潜在的骨干治疗的方案,最终目标是提高乙肝患者的功能性治愈率。”
参考资料:
[1] Spring Bank Pharmaceuticals官网
[2] Spring Bank Pharmaceuticals Announces Positive Top-Line Results from the Second Cohort of Part A of the Phase 2 ACHIEVE Trial
