来自波士顿儿童医院哈佛干细胞研究所的科学家们在小鼠体内获得了一些新的证据,证实通过迫使成熟肝细胞回复到一种干细胞样状态,或许能够修复慢性病变肝脏。
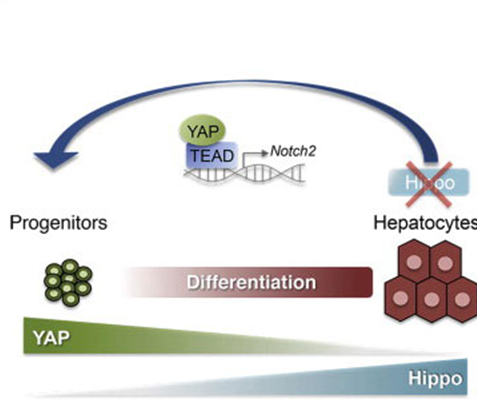
Fernando Camargo领导研究人员调查了一种叫做Hippo的生物化学级联反应,除控制了肝脏的生长大小外,是否还影响了细胞的命运,在此过程中他们偶然获得了这一研究发现。发表在《细胞》(Cell)杂志上的研究结果表明,关闭成熟肝细胞中的Hippo信号通路可导致非常高的去分化率。这意味着这些细胞反转时钟重新变回了干细胞样状态,因此使得它们能够生成一些可再生病变肝脏的功能性祖细胞。
数十年来肝脏都是一种再生模型,众所周知成熟肝细胞可以响应损伤进行复制。即便手术切除四分之三的肝脏,仅凭细胞复制就可以让器官恢复正常的功能大小。这些新研究表明,有第二种再生模式或许可以修复非急剧性的,更为持久的肝损伤,并挑战了长期以来的一2理论:肝脏中存在一个有待激活的干细胞池。
Camargo说:"我认为这项研究阐明了成熟肝细胞巨大的可塑性。你并不是只有非常小的一个细胞群可以招募至损伤处;几乎80%的肝细胞可以经历这种细胞命运转变。"
Cell论文的共同第一作者、波士顿儿童医院的DeanYimlamai博士和Constantina Christodoulou博士完成了大部分的研究工作,阐明了这些转变的生物学,并确定了这些去分化细胞是功能性的祖细胞。
Camargo说,下一步是阐明慢性肝损伤或是诸如肝炎等疾病是如何影响细胞中的Hippo活性变化的。从长远来看,这项研究工作有可能促成一些能够操控患者成熟肝细胞中Hippo活性的药物,刺激去分化并促进愈合。
在这篇Cell论文中,Camargo研究小组利用出生即患一种遗传性肝病的小鼠,探讨了是否有可能通过控制Hippo信号在实验皿中培育出无数的肝祖细胞。他们培育了健康肝祖细胞,将它们移植到患病小鼠体内。在3-4个月的时间内,移植肝细胞被灌注到小鼠体内,它们的疾病有所好转。
Camargo说:"自90年代初期以来,人们一直在设法利用肝细胞移植物来治疗某些代谢疾病,然而由于细胞的来源是被丢弃的肝脏,他们未取得成功。有了来自患者的这种无限的细胞资源,我们认为或许是时候重新思考在肝遗传性疾病情况下进行肝细胞或祖细胞移植。"
在观察到成熟肝细胞去分化之前,去年哈佛大学的研究人员发布了许多相关研究表明,在不同内脏,包括肾脏、肾上腺和肺脏中的一些成熟细胞比原以为的更具可塑性。
Camargo说:"由于这一领域一直以干细胞为中心,这或许是人们忽视了的东西。但我认为我们机体中的细胞具有可塑性这一点非常重要,了解作为这种可塑性基础的信号通路,有可能为操控再生或是扩增用于再生医学的某些细胞类型提供另一种途径。
