治疗失败的处理
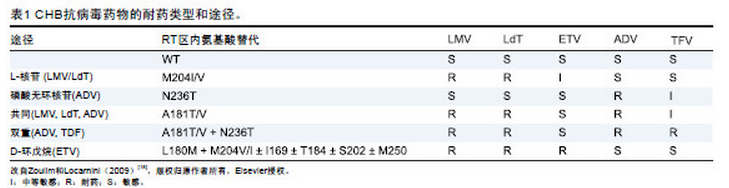
治疗失败的处理在近年来发生了明显的变化。事实上,在出现强效抗病毒药物和病毒学检测手段以后,治疗失败的概念不仅包括经典的病毒学突破,还可以扩展到部分病毒学应答。在任何情况下都应当严格检查治疗依从性,并强调在目前交叉耐药数据(表1)的背景下,根据患者特异HBV pol DNA 序列的耐药谱来处理耐药的必要性。
治疗依从性评估
抗HBV 治疗中依从性良好对维持最大限度抑制HBV 复制非常重要。依从性不佳可导致血清药物浓度明显下降(取决于漏服药物的次数和药物半衰期),并导致病毒载量上升。CHB 患者NA 治疗的依从性研究显示,近40% 的患者未完全依从,明显影响病毒抑制率。ADV 的部分应答也与依从性差有关,当然也与高体重指数等其他药理学参数有关。依从性不佳相关的低水平病毒复制增加了NA 的效力压力,随后会导致耐药风险上升。特异性治疗依从性问卷和血药浓度监测有助于患者的治疗。事实上,HIV 感染者抗病毒治疗的研究已显示,与药物效力与耐药之间的关系类似,依从性和耐药之间也存在一种钟形曲线的关系。来自该研究的数据还提示使用更强效的药物可能使依从性差的患者耐药率降至最低,因为即使依从性水平很低,在接受更强效治疗方案的患者中HIV RNA 可检出率和耐药率也较低。
在临床实践中不易评估治疗的依从性。研究显示,与计数药片或电子监测(MEMS)方式相比,基于自我报告的依从性数据可能虚高。教育水平、健康保险类型、文化因素以及药物低报销率均对药物依从性有统计学意义的影响。所有这些数据提示,为改善临床实践中的抗病毒疗效,对患者进行教育和对药物依从性提供临床上的支持十分重要。
根据交叉耐药调整治疗
交叉耐药定义为由于使用某种药物选择产生改变,使得患者对另一种未使用过的药物耐药(见表1)。由某一种NA 选择出的耐药相关突变对同一结构组的其他药物至少在一定程度上耐药,也可以降低另一化学组NA 的敏感性。初治药物的选择和随后的挽救治疗应当以交叉耐药知识为基础,即第二种药物与第一种治疗失败的药物耐药谱不同。这一点尤其重要,因为被先前治疗选择出的耐药突变株会被储存在肝脏的病毒cccDNA 库中。最近还强调了加用交叉耐药谱不同的NA 联合治疗方案的优势,基于病毒耐药途径的交叉耐药谱总结于表1。加药方案的优势还在于提高了耐药屏障和药物效能,降低了耐药发生的可能性。
耐药的处理
依从性良好的患者发生病毒学突破与病毒耐药有关。以往曾经使用过NA 或初治患者基线HBV DNA 水平高、治疗后HBV DNA 水平下降缓慢,以及部分病毒学应答均与耐药相关。对于耐药患者,应当在ALT 升高之前,通过HBV DNA 水平监测(如有可能,还应当检测耐药基因谱)尽早确定;并以此为基础为患者制定最佳的治疗策略。临床和病毒学研究也证实了早期(在病毒载量上升时即刻)调整治疗的益处。一旦出现耐药,应该以抗病毒最有效,同时发生选择性耐药株风险最小的方案开始挽救性治疗。因此,推荐的方案是加用第二种与先前药物不在同一交叉耐药组的药物(即L- 核苷vs 磷酸无环核苷vs D- 环戊烷)。
尽管加用一种无交叉耐药的药物以防止MDR 株的出现和提高耐药屏障具有很强的病毒学理论依据,然而基于目前相关的临床短期观察,仍倾向于推荐换用一种高耐药屏障且不产生交叉耐药的药物;这一选择目前正在各国家和国际性指南中积极讨论,并且需要通过长期临床和分子病毒学研究的严格评价,才能对这一关键问题下定论。而且,更换药物的策略不适用于经过多种单药治疗的患者,这类患者应当采用加药联合治疗的策略,以最大限度地降低治疗失败的风险。
表1 显示了最常见耐药HBV 变异株的交叉耐药数据。治疗调整应当遵循以下几点原则:
(i)LMV 耐药: 加用TDF( 如无TDF, 加用ADV);也有指南建议更换为TDF ;但由于高耐药率和低药效,不推荐更换为ADV。
(ii)ADV 耐药:推荐更换为TDF(如可行)和加用第二种无交叉耐药的药物。如果以往未使用过LMV,更换为ETV 对ADV 耐药患者也有效。如基因型耐药监测显示rtN236T 替换,考虑LMV 或LdT 联合TDF,或更换为Truvada(TDF 和FTC 的复合制剂);另一方面,如患者先前未使用过LMV,也可更换为ETV。如果存在rtA181V/T 替换, 无论是否合并rtN236T, 均推荐ETV 联合ADV 治疗,或更换为TDF 联合ETV,如患者既往未使用过LMV,也可考虑更换为ETV。
(iii)LdT 耐药:推荐加用TDF(如无TDF,可加用ADV);有些指南中也推荐更换为TDF ;但由于高耐药率和低药效,不推荐更换为ADV。
(iv)ETV 耐药:推荐加用TDF。
(v)TDF 耐药:至今未证实TDF 的原发耐药。建议由参比实验室通过基因分析和/ 或表型分析来确定交叉耐药谱。对于TDF 耐药的患者可加用ETV、LdT、LMV 或FTC,但应以基因分析测定的耐药谱为根据(表1)。
值得注意的是,某些联合方案在长期治疗中的安全性未知,联合治疗并不总是能有效地充分抑制病毒。这些建议是根据“理想世界”的治疗理念作出的,并未考虑费用及药物能否获得。
原发性无应答
原发性无应答和部分应答的处理
可能由于ADV 药效较弱,相比其他NA,原发性无应答在AVD 治疗的患者中更常见(约10% ~ 20%)。对ADV 无应答的患者应当尽早更换为TDF 或ETV 治疗。对LMV、LdT、ETV 或TDF 治疗原发性无应答者罕见;对于这些患者,依从性水平的判断十分重要。对于依从性良好的原发性无应答患者,分析HBV 聚合酶的NA 耐药突变有助进一步治疗(见表1)。
部分病毒学应答
部分病毒学应答可见于使用任何NA 治疗的患者中。依从性的检查对这些患者也十分重要。对LMV、ADV 或LdT 部分病毒学应答的患者有2 种治疗策略:尽早(治疗24 周)更换为一种更强效的药物(ETV 或TDF)或加用一种无交叉耐药的强效药物。介于以上原因,并参照体外研究数据,如果HBV 变异株已经对ADV 耐药(即rtA181T/V ± rtN236T),则不推荐TDF单药治疗,因为这些药物属于同一化学组(磷酸无环核苷类)。当然,还需要更多数据来全面阐释这种情况(具体讨论见下文)。
在TDF 或ETV 部分应答的情况下,推荐更换或最好加用其他药物以达到HBV DNA 在检测水平以下的目标。但这些方案的效果并未经过大型多中心临床研究证实。
持续低病毒血症和病毒载量一过性波动(blips)
持续性极低病毒血症已成为高耐药屏障药物(ETV和TDF)治疗中出现的新问题。事实上,目前实时PCR方法对HBV DNA 的检测下限可达10 ~ 15 IU/mL,而在较早的III 期临床试验中采用的PCR 法检测下限约为60~ 80 IU/mL。在ETV 或TDF 长期治疗过程中,高达5%的初治患者仍维持HBV DNA 阳性。通常来说,如此低水平的病毒血症无法进行包括病毒群序列分析、特异性杂交或克隆分析在内的病毒基因组序列分析。这一现象的临床和生化学意义,尤其是在耐药方面的意义仍不清楚。尽管如此,在人原代肝细胞培养中进行的体外研究和在鸭HBV 模型中进行的体内研究数据均提示,抗病毒治疗中存在病毒血症可导致新细胞感染,并在这些细胞中形成新的cccDNA 分子,从而导致肝脏受感染细胞清除的延迟。
与HIV - 1 感染者在高效抗逆转录病毒治疗中相同,一些HBV 低于检测下限的患者可能会出现短暂的病毒血症。有人认为这一现象提示存在不完全病毒学抑制和/或发生耐药。然而基于HIV 治疗中的经验,多数短暂病毒血症提示患者平均病毒载量低于检测下限,但在生物学和统计学上发生了一定的波动,不太可能提示病毒不完全抑制和/ 或发生耐药。这种短暂的病毒血症与耐药突变无关,也与病毒学或临床治疗失败无关,尤其是在患者接受高耐药屏障药物联合治疗的情况下。
经多种抗病毒药物治疗患者的情况
目前许多患者采用多种抗病毒药物治疗,包括LMV 联合ADV、LMV 和ADV 序贯治疗、甚至再更换为ETV,导致二线或三线治疗药物的选择成为日益显现的问题。而且这种情况下挽救性治疗的效果可能受先前治疗的影响。
在一项欧洲的回顾性多中心研究中,评估了TDF单药治疗对先前各种NA 治疗失败或发生耐药患者的疗效。先前的治疗包括LAM、ADV 和相关序贯及联合治疗。平均治疗23 个月的患者HBV DNA < 400 拷贝/mL(< 60 IU/mL)的总累积比例为79%。LMV 耐药不影响TDF 的疗效,但ADV耐药会影响TDF 的疗效。尽管如此,在整个观察期间患者未出现病毒学突破。
值得注意的是,在一项比较不同治疗对ADV 不完全应答患者疗效的临床试验中,得到的结果与欧洲的研究不同。该研究评估了固定剂量的FTC 和TDF 早期联合(初治联合用药)与TDF 单药治疗的效果。直到治疗24 周(设盲治疗直接比较),两组的病毒水平下降曲线相同。TDF 或TDF 和FTC 复合制剂(Truvada) 治疗48 周时,有81% 的患者HBV DNA 低于检测下限。基线存在LMV或 ADV 相关突变不影响病毒学应答。治疗48 周达到HBV DNA 低于检测下限的主要影响因素是治疗的依从性。相反,近期一项澳大利亚研究分析了对于先前LMV 治疗失败,ADV 治疗至少24 周但病毒仍明显复制的患者(主要为亚裔患者)应用TDF的疗效。治疗48 周和96 周时分别有46% 和64% 的患者HBV DNA 低于检测下限。应答情况与基线LMV 治疗或ADV 耐药无关。然而对一些个案报道的回顾发现,与初治患者相比,基线存在ADV 耐药替换(rtA181Tvs rtN236T ± rtA181T/V)可能影响TDF 治疗的病毒学应答,尤其是对于在基线存在双重突变(rtA181T/V+ rtN236T)的患者(表1),可持续存在较高水平的病毒血症。
对于经各种NA 治疗失败、持续性病毒血症且病情加重的患者,经TDF + FTC(Truvada)联合治疗的临床经验显示该方案抗病毒效果非常好。Kaplan - Meier分析显示联合治疗48 周时HBV DNA 低于检测下限的患者比例为76%,第96 周达94%,无病毒学突破。
重要的是,大多数研究结果显示,TDF 联合LMV 并不比TDF 单药治疗更有效。
欧洲ETV 治疗的临床实践经验显示,只要未出现LMV 耐药(检出rtM204V/I),ETV 对于经LMV 或ADV 治疗患者的病毒抑制效果与在初治患者中相当;不出意外,ADV 耐药不影响ETV 的疗效。有意义的是,ETV 与TDF 的联合治疗已经成功用于因多重耐药治疗失败患者的挽救性治疗。这些结果提示在调整治疗时,应根据治疗史、以往NA 类型和是否存在耐药突变等采用不同的抗病毒策略[ 简单更换为另一种新药或联合两种新药(TDF 或ETV)] 以达到抑制HBV DNA 低于检测下限的目标。

总结
多项临床研究证实,与低耐药屏障药物如LMV、ADV 或LdT 相比,高耐药屏障药物如ETV 和TDF 的耐药率明显较低。一线治疗的正确选择应当包括强效高基因屏障药物,以获得长期持续的抑制病毒复制,从而在最大程度上获得达成首要治疗目标(即防止肝病进展)的机会。大多数患者需要长期接受抗病毒治疗,因此耐药成为主要关注的问题,尤其是在使用低效、低基因屏障药物时。强效、高耐药屏障药物如ETV 或TDF 可以将耐药发生的风险降至最小、维持将来的治疗选择和获得长期治疗成功的最大机会。处理治疗失败的患者需要严格的临床准则和准确的病毒学监测,还需要恰当应用无交叉耐药的互补药物进行早期临床干预(表1)。假如能遵循这些推荐意见,大多数需要抗病毒治疗的CHB患者至少会在中短期内从治疗中受益。对经多种药物序贯治疗的患者,有必要对药物效力和耐药情况进行长期监测。最后,为提高现有抗病毒药物疗效和达到消除HBsAg,甚至期待下一步达到清除HBV 的目的,认识新的治疗目标仍是研究中的主要挑战。
专家点评
上海长海医院 万谟彬教授
经核苷(酸)类似物(NA)治疗患者因耐药导致治疗失败者临床并不少见,对于临床处理我国医生已有一定认识,并积累了较丰富的经验。本文在较全面综述了NA 分类和耐药发生原因并在此基础上提出了治疗失败的处理建议,具有重要参考价值。其中关于治疗失败的主要措施是使用无交叉耐药药物联合疗。这是目前在国际上已经达成的共识,与国际上专业学会的乙型肝炎指南意见基本一致。但其中涉及替诺福韦酯的联合治疗,由于该药在国内尚未面市,并不适合中国国情。国内由于阿德福韦酯价格及来源等因素仍然是联合治疗中的主要药物,其中包括对单药应答不佳或已发生耐药的处理。因此,对于治疗失败的患者仍然建议按照我国慢性乙型肝炎防治指南的推荐建议处理。
