第二军医大学附属长征医院 缪晓辉 赵克开
近年来,乙型肝炎病毒学和免疫学的研究水平得到了很大提高,本报《消化·肝病周刊》特别邀请上海交通大学医学院瑞金医院感染科陆志檬教授担任特约主任编委,由国内专家撰稿,向读者系统介绍乙型肝炎病毒(HBV) 病毒学和免疫学诊断进展。2009年5月21日D2~D3 版介绍了HBV DNA 检测、HBeAg 阴性相关乙肝病毒突变检测,本期D2~D3版继续介绍乙肝病毒cccDNA检测以及HBeAg定量检测。
乙型肝炎病毒cccDNA检测技术介绍
乙肝病毒共价闭合环状DNA (cccDNA)的发现与检测方法的建立始于上世纪80年代,当时米勒(Miller)等采用DNA电泳及Southern 杂交检测技术,证实慢性乙肝患者肝组织内存在一种电泳带位置为2.0 kb 的HBV DNA分子,并在电镜下证实为一种约3.2 kb的超螺旋DNA分子。随着聚合酶链反应(PCR)技术的发展,相关技术开始应用于乙肝病毒cccDNA检测。目前HBV cccDNA的定量检测技术主要有以下3种。
选择性荧光定量PCR
乙肝病毒的松弛环状DNA分子(rcDNA)的正链和负链上均存在缺口,故可设计跨越两个缺口的引物,使rcDNA不会被扩增。同样,对于细胞内以双链线性DNA(dsl-DNA)或单链DNA(ssDNA)形式存在的病毒基因,由于两条引物的方向相反,也不会被扩增。而cccDNA是完整的双链环状结构,故可以被选择性扩增(见图)。
嵌合引物法
嵌合引物由两个片段连接而成,3’ 端的片段A与HBV DNA正链DR2区的序列互补,5’ 端的片段B是与HBV基因组没有同源性的一段序列。引物与正链杂交后,在DNA聚合酶的作用下进行单链延伸。对于rcDNA,由于缺口的存在,引物的延伸停止于DR2区。但如模板为cccDNA,因为正链完整,引物能够顺利延伸形成一条新生链。随后,以第一轮单链延伸形成的产物为模板进行荧光PCR扩增和定量检测。
侵入分析法
侵入分析法的设计也是利用rcDNA正链不完整这一特征,但其使用的是侵入探针技术,而非PCR技术。该方法设计了2个探针,分别为初始探针和侵入探针,前者与正链DR2上游区域的特定序列互补,后者与正链DR2区域的特定序列互补。显而易见,只有正链完整的cccDNA分子,才能同时与两个探针互补。侵入探针的作用是切割初始探针上的一段翼DNA片段,该片段被一个荧光共振能量转移(FRET)盒接受,从而发出荧光信号,进行定量检测。
值得注意的是,上述方法均存在特异性不强的问题。如采用选择性PCR方法,在反应体系中rcDNA模板量较高时,以不完整的两条链为模板形成的单链延伸产物片段之间可以互为引物而出现自身退火,从而形成一定量的扩增产物,导致假阳性结果。而嵌合引物法和侵入分析法则可以扩增dsl-DNA,后者约占全部乙肝病毒基因组的5%~10%。因此,必须高度重视检测方法的特异性,不恰当的检测方法有可能导致错误的结论。
例如,有学者采用套式选择性PCR方法,“证实”外周血单个核细胞内存在cccDNA,显然存在放大选择性PCR“非选择性扩增”的可能。为提高检测的特异性,可采取细胞核抽提技术、沉淀法或酶切法去除rcDNA等措施,以尽可能得到较纯的cccDNA模板。
如何提高cccDNA检测的灵敏度是另一个需要解决的问题。有学者最近提出,可采用滚环扩增技术(RCA)检测cccDNA。实验结果表明,该技术可有效区分rcDNA和cccDNA。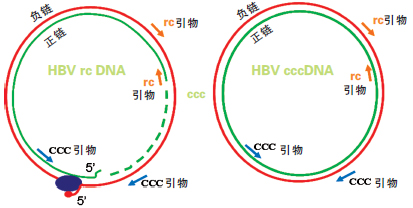 图 HBV cccDNA 的选择性PCR
图 HBV cccDNA 的选择性PCR
HBV cccDNA检测技术的应用
评价慢性乙肝抗病毒治疗疗效
目前考核干扰素和核苷类药物抗病毒效果的标准通常分为主要标准和次要标准。这些标准都是建立在乙肝病毒被抑制或可能被清除的间接评价指标之上,比如,病毒DNA达到不可测水平、HBeAg消失或血清转换、HBsAg消失或血清转换等。鉴于乙肝病毒cccDNA是乙肝病毒在肝细胞内复制的初始模板,而且在肝细胞内的含量相对稳定(每个细胞约5~50 拷贝),因此公认,HBV cccDNA是乙肝病毒难以被清除和停止抗病毒治疗后乙型肝炎复发的分子基础。
只有彻底清除细胞核内的cccDNA,才是真正意义上治愈了乙型肝炎,只要细胞核内的cccDNA被彻底清除,就有理由认为乙肝病毒复制的基础不复存在了。可见,考核抗乙肝病毒药物疗效的指标,或者评价抗病毒治疗的最终疗效标准,应该是清除cccDNA,其他任何指标与之相比只能是“次要”标准。有研究表明,在血清HBsAg被清除的HBV感染者中,肝细胞内仍有cccDNA存在。
清除cccDNA这一过程比较漫长,需要较高的社会、经济成本。此外,在现有条件下进行长期治疗,伴随的必然是药物不良反应的增加以及病毒耐药突变等。因此,是否把清除cccDNA作为治疗终点,还需要进行更多的研究。
筛选抗病毒药物
对抗病毒药物的不断研发,给慢性乙肝患者提供了更多治疗选择。但如前所述,目前的抗病毒药物均不能有效清除cccDNA,因此,开发新的、能清除cccDNA的药物是患者和医生共同的期待。鉴于cccDNA的形成是在细胞核内进行的,因此,能清除cccDNA的药物必须能干预细胞核内cccDNA形成。由于核苷类药物只能干预细胞浆内前基因组RNA逆转录形成病毒DNA负链和以负链为模板进行正链延伸的过程,自然就不能清除cccDNA。
遗憾的是,cccDNA分子在细胞内形成的一些关键环节,目前还不清楚或存在争论,例如:① rcDNA分子究竟是如何通过核转位从细胞浆进入肝细胞核内的?② rcDNA在细胞核内被去掉负链的末端蛋白和正链寡RNA帽是如何实现的?③ 补齐rcDNA两条链的缺口,所需要的DNA聚合酶来自于病毒自身还是宿主?④ cccDNA从环状双链分子进一步折叠形成超螺旋分子,显然需要具有解旋、拓扑异构等生物学活性酶的参与,这些酶是来自病毒还是宿主?上述过程的阐明,将有助于指导开发新的、可能清除cccDNA的抗病毒药物。
评价乙肝病毒复制的模型
一种细胞或动物模型能否支持乙肝病毒复制,cccDNA显然可以作为一个较好的评价指标,因为cccDNA是病毒在细胞内进行复制的初始模板。最典型的例子是HBV转基因小鼠,尽管能检测到rcDNA 和各种病毒抗原蛋白,并且能合成大量的HBV,但在其肝细胞核内未能检测cccDNA,因此,转基因鼠不能作为乙肝病毒感染的动物模型。相反,有学者发现用HBV去感染原代培养的树肝细胞,其细胞核内存在HBV cccDNA,因此,树可能是支持HBV复制的小动物模型。
评价肝组织损伤程度
乙肝病毒cccDNA分子虽存在于肝细胞核内,但从理论上推测,如果乙肝患者变性坏死的肝细胞较多,血清中是完全有可能检测到cccDNA的,而且理论上讲,肝细胞变性坏死越严重(如肝衰竭大面积肝坏死时),外周血中检测到cccDNA的机会也应该越大。
应用于肝移植
HBV cccDNA检测技术在肝移植中的应用至少包括2个方面:即肝脏移植供者的筛查和受者HBV感染或再感染的早期发现。因不排除抗-HBc阳性供体肝脏中存在乙肝病毒可能,有学者主张对受者进行预防性抗病毒治疗,以防止受体感染或再感染HBV。笔者认为,完全可以对此类供体进行肝内cccDNA检测,如阴性则没有必要进行过度的预防性抗病毒治疗。同样,如受者原为HBV感染者,也可以定期对其肝组织进行HBV cccDNA检测,判断肝细胞内有无乙肝病毒复制,以便在血液中出现大量病毒之前早期发现HBV感染或再感染,甚至有可能指导抗病毒药物的使用疗程和乙肝免疫球蛋白剂量的调整。关于cccDNA检测技术在肝移植中的应用,还有待于进一步临床研究。
责任编辑 杜佳梅
